Los hidruros son compuestos químicos que combinan átomos de hidrogeno y átomos de cualquier otro elemento que podamos encontrar en la tabla periódica. En pocas palabras, se forman con la combinación del hidrógeno con otro elemento.
¿Qué es?
Los hidruros son compuestos químicos que constan de cualquier elemento químico e hidrogeno. Se clasifican en: Hidruros metálicos, si se forman con un metal y un hidrogeno, teniendo un estado de oxidación de -1; e hidruros no metálicos, que se forman por la unión de un no metal y un hidrogeno y tienen un estado de oxidación de +1.
¿Cómo se forman los hidruros?
Se forman de manera muy sencilla a través de la combinación de cualquier elemento con hidrogeno. Debido a que el hidrogeno es un componente muy común en diversos materiales, podemos decir que están en todas partes. Sin ir más lejos, el agua es un hidruro, los alimentos cuentan con enlaces de carbono e hidrógeno, los plásticos, la ropa y muchos compuestos más son hidruros.
Nomenclatura
La nomenclatura varía según se hable de hidruros metálicos y no metálicos. En el caso de estos últimos, el no metal siempre actuara con su menor número de valencia, por lo que cada uno de ellos solo formará un hidruro no metálico a temperatura ambiente.
En este caso, se formulan escribiendo el símbolo del hidrogeno y luego el elemento, luego se intercambian las valencias. El hidrogeno siempre actúa con su valencia +1 mientras que los no metales del grupo 17 como el flúor, cloro, bromo y yodo actuarán con valencia-1. Los no metales del grupo 16 como el azufre, selenio y telurio actuarán con valencia –2.
Para nombrarlos se le añade la terminación uro en la raíz del nombre del no metal y luego especificamos el hidrogeno. En el caso que a sustancia se encuentre en disolución acuosa, se considera un ácido y pasan a utilizar la terminación –hídrico:
H2S: Sulfuro de hidrógeno/ácido sulfhídrico.
H2Se: Seleniuro de hidrógeno/ácido selenhídrico.
H2Te: Telururo de hidrógeno/ácido telurhídrico.
HBr: Bromuro de hidrógeno/ácido bromhídrico.
HCl: Cloruro de hidrógeno/ácido clorhídrico.
HF: Fluoruro de hidrógeno/ácido fluorhídrico.
HI: Yoduro de hidrógeno/ácido yodhídrico.
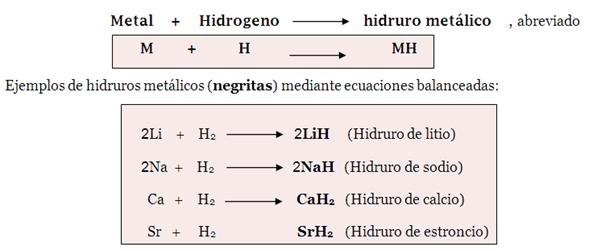
En el caso de los hidruros metálicos, tenemos que se formulan escribiendo primero el símbolo del elemento metálico. Se nombran por la palabra hidruro seguida del nombre del metal. En caso que el metal cuente con más valencias se emplean los sufijos ico y oso para la menor y la mayor respectivamente. Si encontramos más de dos valencias, se emplearán además los prefijos Per e Hipo según sea necesario.
Características
Entre las principales características de los hidruros tenemos:
- Son térmicamente inestables y pueden explotar en presencia de aire o humedad.
- Los hidruros no metálicos tienen como número de oxidación del hidrógeno el 1.
- Los hidruros metálicos tienen como número de oxidación del hidrógeno -1.
- Dependiendo del elemento con el que se combina, el hidrogeno de los hidruros formara enlaces iónicos o covalentes.
- Se les cataloga como como compuestos inorgánicos binarios, esto se debe a que tienen dos elementos químicos.
- Son catalogados porque tienen dos elementos químicos.
Usos y aplicaciones
Entre los diferentes usos de los hidruros podemos mencionar:
- Funcionan como desecantes y reductores.
- Algunos se pueden utilizar como fuentes de hidrógeno puro.
- Son utilizados en baterías recargables de uso doméstico e industrial.
- Se utilizan para la limpieza, en la lavandería y la peluquería.
- Se emplean como plaguicidas para fumigar comercios.
- Se emplean para fabricar explosivos, colorantes de plástico, baterías, fibras textiles, pinturas y abonos.
- Algunos se utilizan en la síntesis de los compuestos orgánicos e inorgánicos del yodo.
- Pueden emplearse en medicina como suplementos.
With a passion for knowledge and a commitment to delivering quality information, Curioso Admin leads our team in curating engaging articles across various domains. Holding a wealth of experience in content creation and a keen understanding of the ever-evolving digital landscape, Curioso Admin is the guiding force steering Curiosos.co to new heights.